www.canva.com
KAPASITAS KALOR GAS
Kapasitas kalor merupakan kalor yang
diperlukan untuk menaikkan suhu suatu zat sebesar 1 kelvin. Secara matematis
kapasitas kalor dirumuskan :

Q = energi kalor (joule)
C = kapasitas kalor (J/K)
∆T = kenaikan suhu (K)
Kapasitas kalor ada dua macam yaitu :
- Kapasitas kalor pada volume tetap (Cv)
- Kapasitas kalor pada tekanan tetap (Cp)
Karena volume tetap, maka usaha sistem = 0, seluruh panas yang diterima sistem sepenuhnya digunakan menaikkan energi dalam sistem, sedangkan panas yang dilepaskan oleh sistem akan menurunkan energi dalam sistem.

Untuk gas monoatomik : ∆U = 3/2 nR∆T

Untuk gas diatomik : ∆U = 5/2 nR∆T

2. KAPASITAS KALOR TEKANAN TETAP (CP)
Pada proses isobarik usaha yang dilakukan gas adalah : W = P ∆V, sehingga kenaikan energi dalam sistem :

Untuk gas monoatomik :




3. KONSTANTA LAPLACE (γ)
Untuk gas monoatomik :

Untuk gas diatomik :

4. HUKUM II TERMODINAMIKA
Hukum II Termodinamika memberikan batasan-batasan terhadap perubahan energi. Hukum Kekekalan Energi yang dinyatakan dalam Hukum I Termodinamika menyatakan bahwa energi dapat diubah dari satu bentuk ke bentuk lain. Misalnya, perubahan usaha (energi potensial) menjadi energi kalor atau sebaliknya. Akan tetapi, tidak semua perubahan energi yang terjadi di alam ini prosesnya dapat dibalik seperti pada Hukum I Termodinamika. Misalnya panas dapat berpindah dari benda panas ke benda yang dingin. Tapi proses kebalikannya tidak mungkin terjadi. Artinya tidak pernah ada panas berpindah dari benda dingin ke benda panas.
Hukum II Termodinamika memberikan batasan-batasan terhadap perubahan energi yang mungkin terjadi dengan beberapa perumusan.
- Tidak mungkin membuat mesin yang bekerja dalam satu siklus, menerima kalor dari sebuah reservoir dan mengubah seluruhnya menjadi energi atau usaha luas (Kelvin Planck).
- Tidak mungkin membuat mesin yang bekerja dalam suatu siklus mengambil kalor dari sebuah reservoir rendah dan memberikan pada reservoir bersuhu tinggi tanpa memerlukan usaha dari luar (Clausius).
- Pada proses reversibel, total entropi semesta tidak berubah dan akan bertambah ketika terjadi proses irreversibel (Clausius).
Mesin carnot (mesin panas/kalor) merupakan mesin yang dapat mengubah energi panas menjadi energi mekanik. Salah satu contohnya adalah mesin diesel yang digunakan pada kendaraan bermotor, mesin uap, dan mesin pesawat. Masih ingat dong MotoGP Mandalika pertama di Indonesia dimana para pembalap mencoba sirkuit yang cukup susah ditaklukkan sampe pembalap kesayangan admin Marc Marquez mengalami kecelakaan yang cukup parah. Ehhh kok jadi bahas MotoGP hehehe.. Nah good learner mesin motor balap juga merupakan contoh mesin kalor. Hasil pembakaran dari bahan bakar diubah menjadi energi gerak dalam mesin motor.
Konsep mesin Carnot ditemukan oleh Nicolas Leonard Sadi Carnot. Mesin Carnot memanfaatkan prinsip kalor yang mengalir dari suhu tinggi ke suhu rendah tanpa perlu melakukan usaha. Saat aliran kalor terjadi, panas yang mengalir diubah menjadi usaha, misalnya gerak.
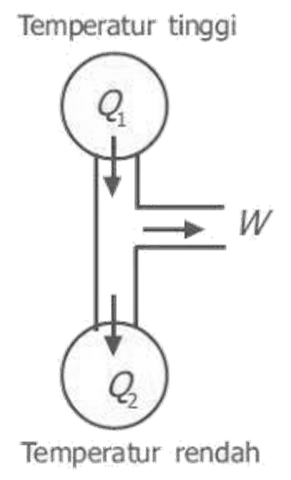
SIKLUS CARNOT

- Proses 1 adalah pemuaian isotermal pada suhu T1. Pada proses ini sistem menyerap kalor Q1 dari reservoir bersuhu tinggi T1 dan melakukan usaha W.
- Proses 2 adalah pemuaian adiabatik (tidak ada panas yang keluar dari sistem) Selama proses ini berlangsung suhu sistem turun dari T1 menjadi T2 sambil melakukan usaha W.
- Proses 3 adalah pemampatan isotermal pada suhu T2. Pada proses ini sistem menerima usaha W dan melepas kalor Q2 ke reservoir bersuhu rendah T2.
- Proses 4 adalah pemampatan adiabatik. Selama proses ini suhu sistem naik dari T2 menjadi T1 akibat menerima usaha W.

Efisiensi mesin Carnot (η)
Merupakan
perbandingan kerja/usaha yang dilakukan oleh mesin dengan panas yang diserap
selama siklus. Efisiensi panas dapat diartikan “berapa bagian panas yang
diterima dapat dimanfaatkan”. Secara
matematis dapat ditulis :

atau

Suatu mesin panas akan mempunyai efisiensi 100 % jika Q2 = 0 yaitu ketika tidak ada panas yang terbuang, seluruh panas yang diterimanya diubah menjadi kerja mekanik. Namun hal ini tidak mungkin terjadi, tidak ada reservoir bersuhu 0 K karena kebanyakan reservoir berada dalam suhu kamar. Sehingga efisiensi mesin selalu lebih kecil dari 100 %. Efisiensi mesin pada umumnya 20 – 40 %.
contoh soal 1 :
Suatu mesin uap bekerja pada suhu 200 ⁰C. Mesin ini mengubah air menjadi uap yang akan menggerakkan piston sehingga menghasilkan kerja mekanik. Suhu di luar mesin 27 ⁰C. Hitung efisiensi panas maksimum dari mesin uap ini ! Hitung juga berapa usaha maksimum yang dapat dikerjakan oleh mesin itu jika ia menyerap panas 500 J.
jawab :
Diketahui :
T1 = 200 + 273 = 473 K
T2 = 27 + 273 = 300 K
Q1 = 500 J
ditanya :
𝜼 = ...?
W = ...?
a. Efisiensi mesin :
Usaha maksimum yang dilakukan gas :

contoh soal 2 :
Efisiensi tertinggi dari suatu mesin uap adalah 40 % yaitu dengan menggunakan siklus carnot. Jika mesin uap ini melepaskan gas ke udara yang suhunya 300 K, berapa suhu dalam silinder gas setelah terjadi pembakaran. Jika mesin panas uap ini menyerap panas sebanyak 800 J tiap siklus, hitung berapa banyak kerja yang dilakukan oleh mesin tiap siklus ?
jawab :
Diketahui :𝜼 = 40 % = 0,4
T2 = 300 K
Q1 = 800 J
ditanya :
T1 =...?
W = ...?


6. MESIN PENDINGIN
merupakan mesin yang berfungsi mendinginkan ruangan dengan memindahkan panas dari suatu ruangan ke ruangan lain. Untuk memindahkan panas dari tempat dingin ke tempat panas dibutuhkan usaha luar. Kenapa perlu usaha? Ini karena proses pada mesin pendingin adalah tidak spontan. Contoh mesin pendingin adalah kulkas, dan penyejuk ruangan (AC). Usaha yang dibutuhkan untuk menjalankan mesin pendingin dapat dihitung menggunakan persamaan.


Jika mesin pendingin itu ideal, maka persamaan yang berlaku adalah :
Pada mesin panas kita mengenal efisiensi mesin, pada mesin pendingin kita mengenal istilah koefisien performance 𝜼p. Koefisien performance didefenisikan sebagai perbandingan banyaknya panas Q2 yang dapat dikeluarkan dari ruang dingin dengan kerja W yang dilakukan kompresor.
jawab :
T2 = 273 - 4 = 269 K
T1 = 273 + 25 = 298 K
W = 200 J
t = 10 menit = 600 s
mesin berdaya 200 watt artinya : setiap detik mesin melakukan kerja sebesar 200 J. Untuk menghitung panas yang diserap Q2 dari mesin pendingin kita hitung dulu kalor yang diserap Q2 dengan rumus koefisien performance :

maka dalam 10 menit kalor yang diserap mesin pendingin adalah :

contoh soal 2 :
Suhu di dalam ruangan suatu mesin pendingin ( kulkas ) 0 ⁰C dan suhu luar 27 ⁰C. Setiap jam panas yang diserap dari ruangan adalah 6 x 10⁶ joule.
a) berapa watt daya listrik yang dipakai untuk menggerakkan mesin kulkas ini
b) Jika biaya listrik Rp 150,00 per Kwh, berapa biaya yang harus dibayar pemilik kulkas setiap hari pemakaian
jawab :
T2 = 273 + 0 = 273 K
T1 = 273 + 27 = 300 K
Q2 = 6 x 10⁶ joule (tiap jam)

(b) Biaya listrik :
daya listrik 165 watt, jika dipakai dalam sejam maka energi yang terpakai (165) x (1jam) = 165 watt jam = 0,165 kWh
biaya : 0,165 x 150 x 24 jam = Rp 594,00
Hello good learner, apa kabar nih ? Sebelumnya admin studygramfisika mau ngucapin minal aidin walfaidzin mohon maaf lahir dan batin kepada semua pembaca blog ini. Dikarenakan libur lebaran admin jadi jarang ngepost hehehe.. Nah hari ini studygramfisika sharing lanjutan materi termodinamika. Catatan termodinamika part 2 ini membahas mengenai kapasitas kalor dan juga hukum termodinamika 2, prinsip kerja mesin kalor dan mesin pendingin. Semoga catatan ini bisa menjadi pelengkap catatan kalian disekolah ya khususnya adik-adik kelas 11 SMA. Selamat belajar 😊
Nah good learner yang mau memiliki catatan ini bisa download di bawah ini.. Jangan lupa sekalian trakterr admin biar terus semangat bikin catatannya hehhe
Trakteer admin here : Link Teer












0 Komentar